
在拉曼影像监控下智能手机激活的感染性角膜炎快速诊疗一体化研究。
细菌感染已成为威胁人类健康的关键原因之一,尤其是耐药菌的不断出现和新型抗生素研发的滞后。例如,耐药菌感染性角膜炎已经成为我国主要致盲性疾病之一。
基于纳米银的抗菌策略最近引起了广泛关注,它可以与光子结合诱导多模式抗菌治疗,如光热疗法(PTT)、 光动力疗法(PDT)、光催化疗法和化学动力疗法。但越来越多的研究表明,纳米银的过度释放游离Ag+会导致细胞毒性。
并且当PDT和PTT通常采用近红外激光激发治疗脆弱组织感染,如眼睛和皮肤时,应仔细检查光源的安全性和适用性。因此,针对耐药细菌的生物相容性、高效且准确的银基抗菌策略仍然具有挑战性。
另一方面,准确检测感染部位的病原菌可以提供有关治疗反应的关键信息。然而,标准菌落计数技术、生物化学鉴定和聚合酶链式反应 (PCR),非常耗时,并且无法提供整个受感染组织的概览。最近新兴的诊断技术中 表面增强拉曼散射 (SERS) 成像是一种高度灵敏且功能强大的分析工具,能够快速、非侵入性地检测细菌及其生物过程。因此,开发高度敏感和特异性的新技术实现早期、精准诊断细菌性角膜炎及新型抗菌策略,用来有效治疗耐药菌并干预其感染进程,是我们角膜炎治疗领域的重大社会需求,对提升难治性感染性角膜炎具有非常重要的科学意义和社会发展需要。
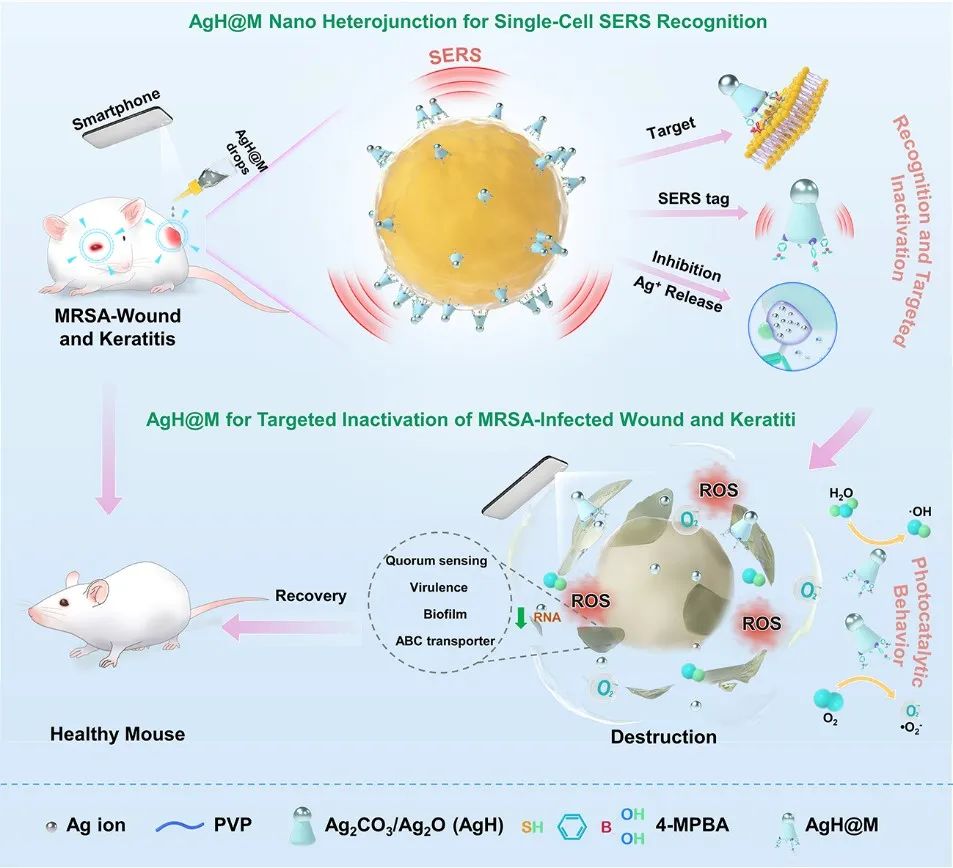
图1:银基纳米异质结(AgH@M)用于诊断与治疗
耐药菌感染角膜炎与皮肤病
为此,浙江大学周民研究员团队联合浙大二院眼科中心、浙江大学眼科医院姚克教授与陈祥军研究员团队在国际知名期刊Nano today(IF: 17.4)在线发表题为“Smartphone-Triggered Targeted Inactivation of MRSA under SERS Monitoring”的研究论文。该课题报道了4-巯基苯硼酸(4-MPBA)修饰的Ag2CO3/Ag2O纳米异质结(AgH@M),它可以在智能手机白光照射下实现单细胞SERS识别并通过开启光催化过程有效根除MRSA。AgH@M 可以同时执行多种功能,包括 MRSA 靶向、拉曼探针分子以及通过 4-MPBA 分子抑制过量银离子释放。此外,感染部位的残留细菌被AgH@M点亮并在体外和体内进行长达7天的实时监测。我们进一步证明,由于充分利用有限释放的Ag+靶向注射到MRSA中,AgH@M对MRSA感染角膜炎取得了令人满意的治疗效果,并且在生物安全性方面具有显着优势。最后,潜在的抗菌机制涉及光催化行为的活性氧(ROS)的大量产生以及群体感应相关基因、毒力相关基因、生物膜相关基因和ATP结合(ABC)转运蛋白相关基因的下调。

图 2 :AgH 纳米异质结结构表征
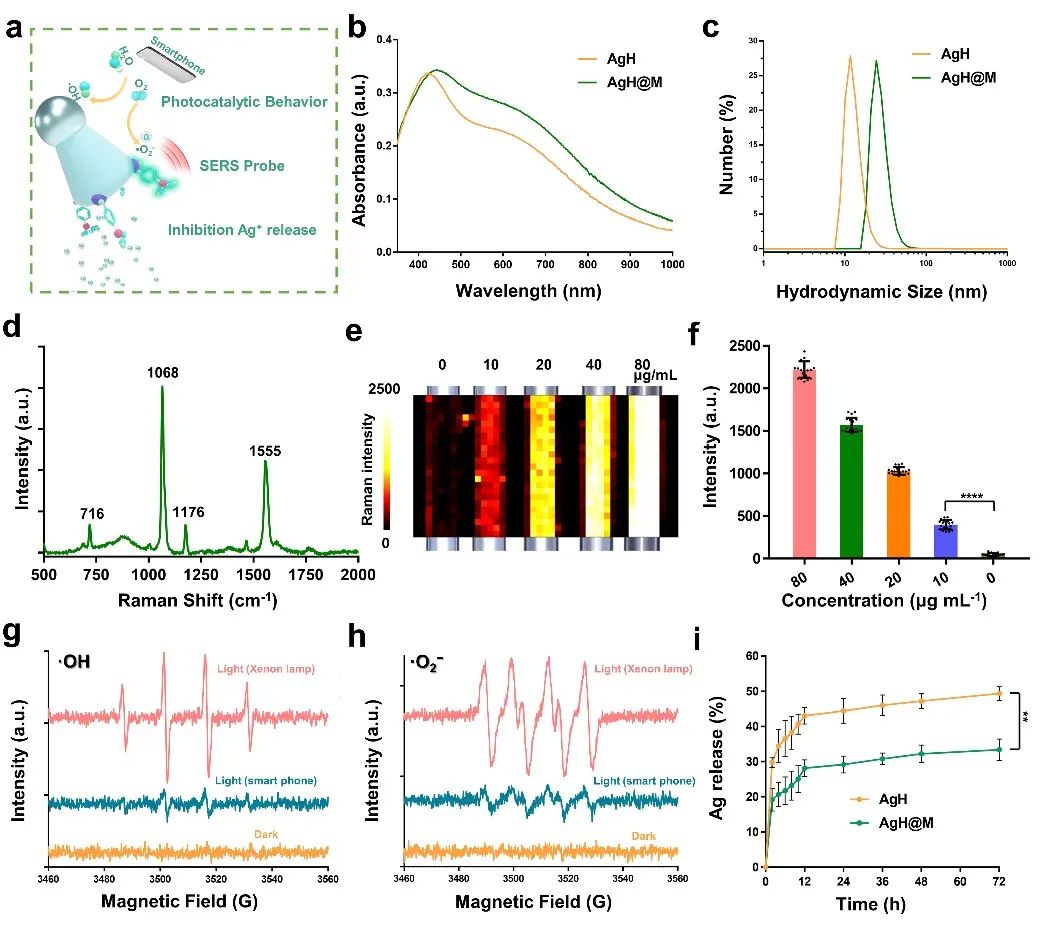
图 3 :AgH@M 表面增强拉曼(SERS)功能
与智能手机激发下的光催化行为
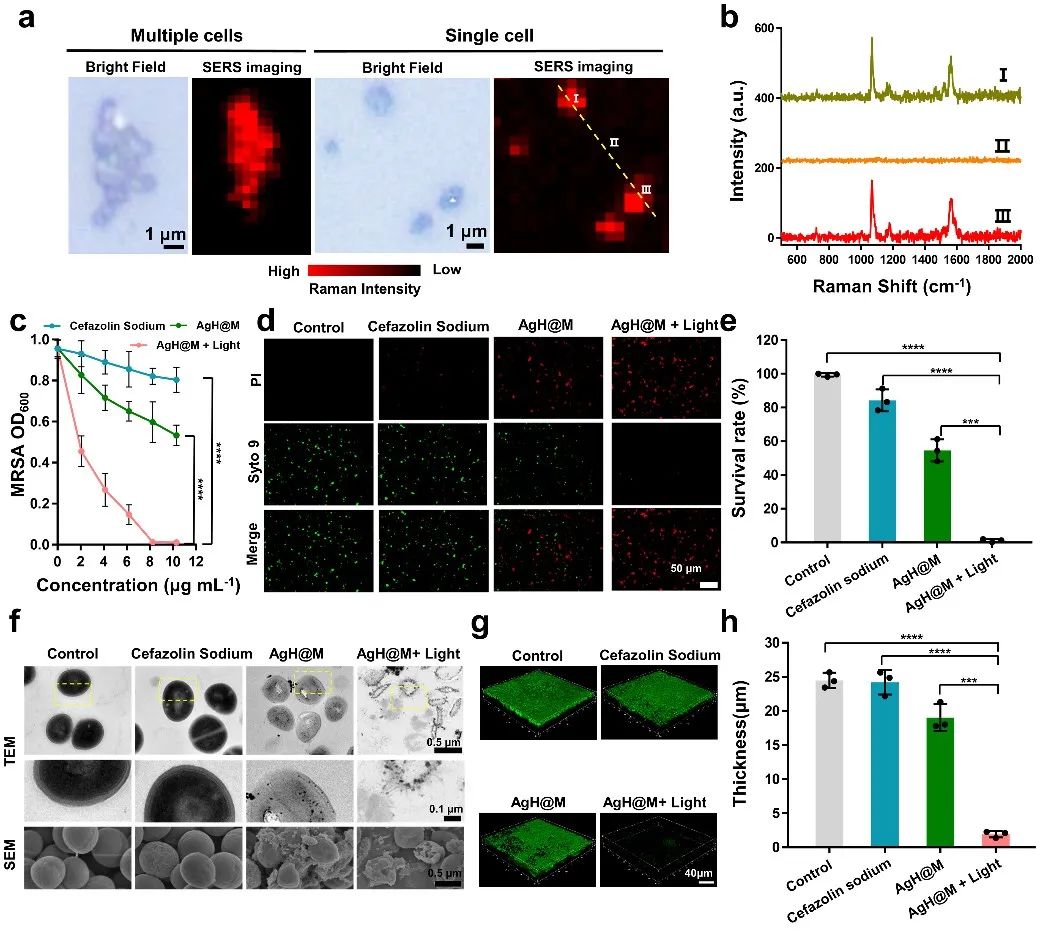
图 4 :单个细菌 SERS 识别及光激活抗菌
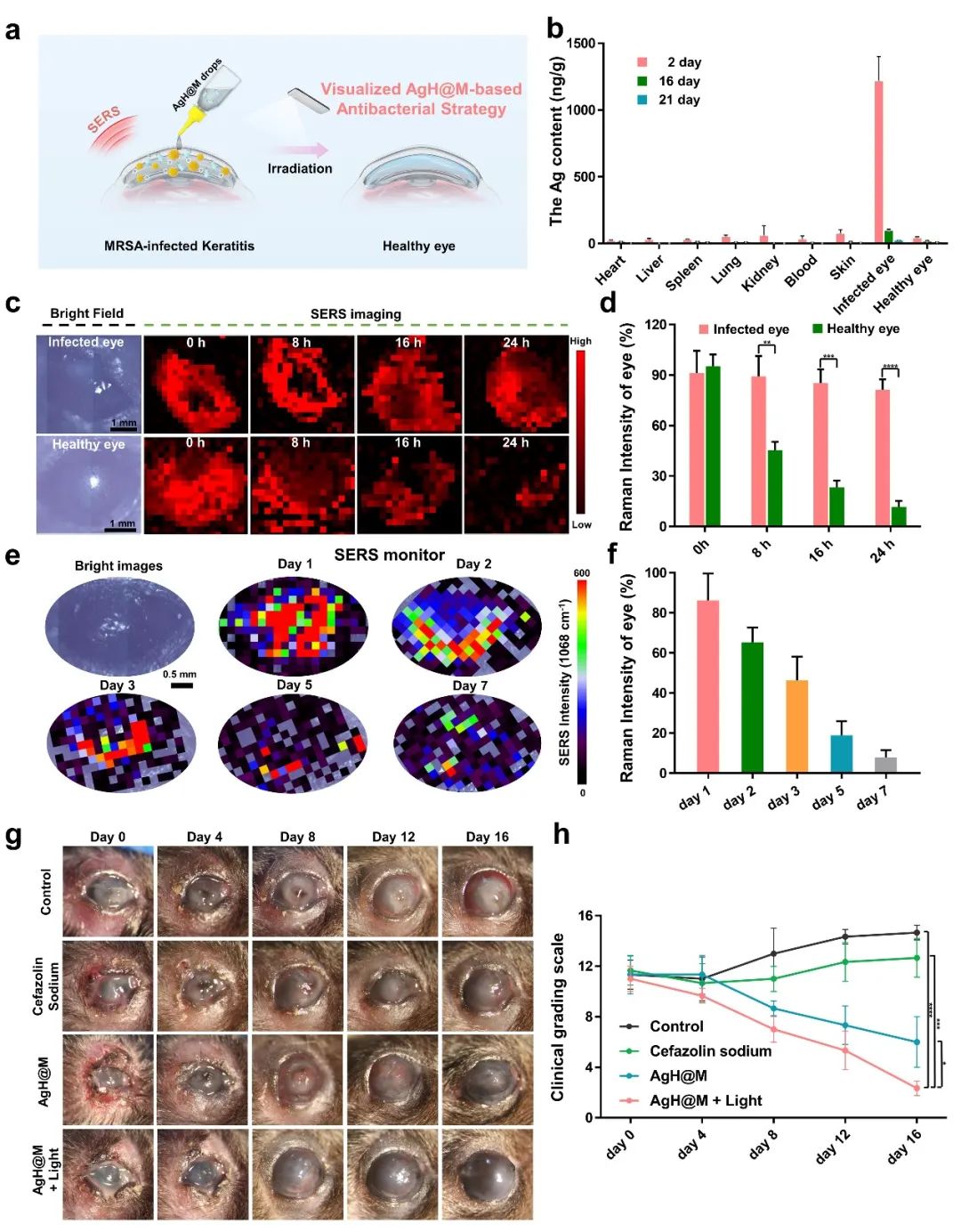
图5 :SERS 影像监控下的细菌性角膜炎的
监控与治疗
浙江大学转化医学研究院博士生何健,浙大二院眼科中心博士生叶洋为本文的第一作者与共同第一作者。浙江大学周民研究员、浙江大学医学院附属第二医院眼科中心、浙江大学眼科医院姚克教授与陈祥军研究员为论文的共同通讯作者。上述研究得到了国家重点研发计划、国家自然科学基金、浙江省重点研发计划项目基金、创新研究院医药转化项等基金项目的大力支持。
在发展新型的耐药菌抗菌策略方面,近年来,周民研究员团队联合姚克教授团队针对细菌性角膜炎,眼内炎等眼科耐药细菌感染疾病,难治性真菌性角膜炎,以及耐药菌感染的肺炎与难愈合伤口,设计了多种新型抗菌剂与策略,特别是设计的铜源眼用纳米凝胶抗菌手段,已经开展相关临床试验,并且取得了满意的临床抗菌效果(Nano Today 2023; ACS Nano 2023; Adv. Mater. 2022;ACS Nano 2022; Nano Today 2022;ACS Appl. Mater. Interfaces 2022; ACS Nano 2021; Bioact. Mater. 2021; Biomaterials 2021;ACS Nano 2020; Theranostics 2020; Appl. Mater. Interfaces 2019; Appl. Mater. Interfaces 2018;)。
论文链接:
https://doi.org/10.1016/j.nantod.2023.102012